Carcinoma esofageo squamocellulare
Pubblicato il 16/09/2014
TITOLO
Risposta obiettiva completa di un carcinoma squamocellulare dell’esofago a terapia biologica
Parole chiave:
carcinoma esofago, risposta obiettiva completa, terapia biologica
Autore
Dr. Giuseppe Di Bella
Ente o istituzione di appartenenza
Fondazione Di Bella – Bologna – Italia
Indirizzo per corrispondenza e-mail: posta@giuseppedibella.it
Telefono 051 239662 ; 051 230369 ; - Fax 051 2961238
Indirizzo postale Via Marconi N°51 CAP 40122 Bologna - Italia
Abbreviazioni
Magnetic Resonance Imaging (MRI)
Positron Emission Tomography (PET)
Growth Hormone (GH)
Epidermic Growth Factor (EGF)
Fibroblastic Growth Factor (FGF)
Insulin-like Growth Factor 1-2 (IGF1-2)
ABSTRACT
L’impiego sinergico di Somatostatina, Melatonina, Retinoidi, Vitamine C, D3, E, Calcio, Amminoglucidi solforati, dosi minime di ciclofosfamide per os, in un uomo di 70 anni con carcinoma esofageo scarsamente differenziato inoperabile, hanno consentito, dall’inizio della cura nel 1995, ad oggi, una qualità di vita eccellente, e la guarigione con recupero funzionale.
Vengono discussi il razionale e i meccanismi d’azione molecolare della terapia, che esercita un effetto antiproliferativo, differenziante, apoptotico, preservando ed esaltando, al contrario della chemio e/o radioterapia, sia il trofismo e la funzionalità di organi e tessuti , che l’omeostasi immunitaria e antiblastica.
Questo risultato, in assenza di tossicità, documenta l’efficacia di questa multiterapia biologica (MDB) ed è conforme ai positivi risultati già pubblicati sull’uso del MDB nei LNH a basso grado e carcinomi polmonari al 3° e 4° stadio.
Il MDB, senza necessità di ricovero, in assenza di tossicità e senza ridurre minimamente l’attività lavorativa, ha progressivamente e lentamente ridotto e poi eliminato la massa tumorale, ottenendo una risposta obiettiva completa.
Riteniamo utile segnalare il caso per invitare ad un maggiore interesse , studio e approfondimento sulle possibilità aperte in oncologia dalla terapia biologica e recettoriale MDB.
Vengono discussi il razionale e i meccanismi d’azione molecolare della terapia, che esercita un effetto antiproliferativo, differenziante, apoptotico, preservando ed esaltando, al contrario della chemio e/o radioterapia, sia il trofismo e la funzionalità di organi e tessuti , che l’omeostasi immunitaria e antiblastica.
Questo risultato, in assenza di tossicità, documenta l’efficacia di questa multiterapia biologica (MDB) ed è conforme ai positivi risultati già pubblicati sull’uso del MDB nei LNH a basso grado e carcinomi polmonari al 3° e 4° stadio.
Il MDB, senza necessità di ricovero, in assenza di tossicità e senza ridurre minimamente l’attività lavorativa, ha progressivamente e lentamente ridotto e poi eliminato la massa tumorale, ottenendo una risposta obiettiva completa.
Riteniamo utile segnalare il caso per invitare ad un maggiore interesse , studio e approfondimento sulle possibilità aperte in oncologia dalla terapia biologica e recettoriale MDB.
INTRODUZIONE
Si presenta un caso di remissione completa (RC) con terapia biologica (MDB) di un carcinoma esofageo monitorato dal 1995 ad oggi. Sono riportati i componenti della terapia biologica MDB (Metodo Di Bella) e una sintesi della documentazione, prima e dopo il trattamento MDB.
Si descrive in estrema sintesi il razionale del MDB, documentandone le basi scientifiche, i meccanismi d’azione di biologia molecolare, la risposta clinica, il favorevole profilo tossicologico.
Il carcinoma esofageo
La prognosi nei pazienti con cancro dell'esofago è sfavorevole, meno del 5% sopravvive a 5 anni (Harrison ). L'escissione chirurgica di tutto il tessuto neoplastico macroscopicamente visibile (resezione totale) è possibile solo nel 45% dei casi, e si associa ad una rilevante percentuale di complicazioni e/o mortalità .
La sopravvivenza a lungo termine è raggiunta solo nei pazienti con tumore che coinvolge meno di 5 cm. dell'esofago e che non hanno né ostruzione, né diffusione extraesofagea (T1NoMo). I pazienti con carcinoma esofageo raramente rispondono a questi criteri. La maggior parte dei pazienti muore per la malattia entro 10 mesi dalla diagnosi. L’associazione della terapia radiante (da 5500 a 6000 cGy) con mono o polichemio può conseguire un'apprezzabile, ma temporanea, riduzione della massa tumorale, penalizzata da rilevante tossicità, ma gli studi clinici randomizzati, finora condotti, non hanno evidenziato la capacità di chemio e/o radioterapia di incrementare significativamente la mediane di sopravvivenza.
CASO CLINICO : carcinoma esofageo (classificazione:T4N2Mx)
Profilo anagrafico del paziente:
Anno di nascita : 1924
Luogo di nascita : Roma
Sesso : M
Professione: Pensionato (ex Geometra)
ANAMNESI —Il paziente M.D. (età 70 anni circa) inizia (da circa 3 mesi) ad accusare disfagia, accompagnata da senso di bruciore in regione retro-sternale e presenza di dolore di media entità irradiato a tutta la regione addominale della durata di alcuni minuti e più volte durante la giornata. Rigurgiti alimentari e calo ponderale (6 Kg./3 mesi). Riferisce inoltre cambiamento dell’alvo tendenzialmente stitico nell’ultimo mese.
ANAMNESI REMOTA - Pleurite all’età di 10 anni, a 21 anni frattura della base cranica, clavicola dx e perforazione timpano dx in seguito ad incidente motociclistico. Broncopolmonite bilaterale all’età di 30 anni , all’età di 31 anni esoftalmo occhio sx per ipertiroidismo. Dall’età di 50 anni circa affetto da ipertensione arteriosa 180/110 mm/Hg trattata farmacologicamente a domicilio.
Inizia accertamenti del caso:
2/3/1995—ANGIO TC Torace Addome rivela…“ispessimento delle pareti del terzo distale dell’esofago toracico e della giunzione esofago-gastrica con presenza di manifestazione diverticolare . Linfonodi di 1 cm in sede pericardiale ed a livello della gastrica sinistra. ..”” Il paziente viene ricoverato c/o III Clinica Chirurgica — Pol. “Umberto I” - Roma
3/3/1995— Eseguito EGDS “ ...a 36 cm. dall’arcata dentaria superiore è presente un diverticolo con ampio colletto (si esegue biopsia) contenente residui alimentari…”
28/3/1995—Istologico: Carcinoma scarsamente differenziato superficialmente ulcerato
4/4/1995- TAC
Anno di nascita : 1924
Luogo di nascita : Roma
Sesso : M
Professione: Pensionato (ex Geometra)
ANAMNESI —Il paziente M.D. (età 70 anni circa) inizia (da circa 3 mesi) ad accusare disfagia, accompagnata da senso di bruciore in regione retro-sternale e presenza di dolore di media entità irradiato a tutta la regione addominale della durata di alcuni minuti e più volte durante la giornata. Rigurgiti alimentari e calo ponderale (6 Kg./3 mesi). Riferisce inoltre cambiamento dell’alvo tendenzialmente stitico nell’ultimo mese.
ANAMNESI REMOTA - Pleurite all’età di 10 anni, a 21 anni frattura della base cranica, clavicola dx e perforazione timpano dx in seguito ad incidente motociclistico. Broncopolmonite bilaterale all’età di 30 anni , all’età di 31 anni esoftalmo occhio sx per ipertiroidismo. Dall’età di 50 anni circa affetto da ipertensione arteriosa 180/110 mm/Hg trattata farmacologicamente a domicilio.
Inizia accertamenti del caso:
2/3/1995—ANGIO TC Torace Addome rivela…“ispessimento delle pareti del terzo distale dell’esofago toracico e della giunzione esofago-gastrica con presenza di manifestazione diverticolare . Linfonodi di 1 cm in sede pericardiale ed a livello della gastrica sinistra. ..”” Il paziente viene ricoverato c/o III Clinica Chirurgica — Pol. “Umberto I” - Roma
3/3/1995— Eseguito EGDS “ ...a 36 cm. dall’arcata dentaria superiore è presente un diverticolo con ampio colletto (si esegue biopsia) contenente residui alimentari…”
28/3/1995—Istologico: Carcinoma scarsamente differenziato superficialmente ulcerato
4/4/1995- TAC
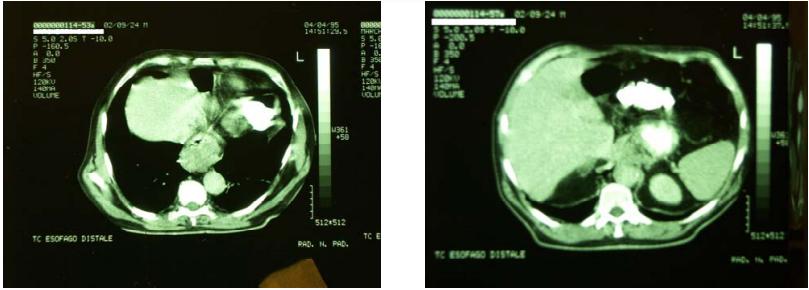
19/4/1995– Viene sottoposto a “Laparotomia esplorativa” con l’intento di posizionare un Port-a-cath utile a consentire una infusione continua di trattamenti chemioterapici ed inoltre valutare l’eventuale possibilità di endoprotesi.
L’esito dell’intervento è palliativo e accerta l’impossibilità di exeresi chirurgica della neoplasia.
Referto della laparotomia esplorativa:- “..voluminosa neoplasia esofagea…che invade il tessuto periesofageo ed il diaframma e si diffonde a caduta nel retroperitoneo , sullo stomaco e al pancreas che vi aderisce strettamente. Nel mediastino si palpano e si dimostrano grossolane gittate verosimilmente neoplastiche. Molti linfonodi regionali ed extraregionali sono aumentati di volume.” Considerando la gravità della diffusione locale, toraco-addominale della neoplasia, l’età e le condizioni generali del paziente, si rinuncia a proseguire l’intervento...”
Viene sottoposto a trattamenti combinati chemioterapici, con riduzione della massa valutabile intorno al 50% (8 cicli 5 FU + mitomicina - 28 cicli radioterapici )
In data 28/10/1995 il trattamento viene sospeso a causa di sanguinamento e melena, e non viene ritenuto possibile ripetere i trattamenti chemioterapici e viene dimesso consigliando unicamente una terapia antidolorifica e di supporto. Progressione tumorale.
Dicembre 1995: Progressione tumorale e inizio MDB
4/4/96—Viene ricoverato per una Broncopolmonite Basale dx .all’Ospedale “Forlanini” di Roma.
Diagnosticata una Cardiopatia degenerativa con insufficienza mitralica lieve.
2/5/96— Viene dimesso, dopo i trattamenti del caso.
3/4/97—TAC di controllo evidenzia una: “complessiva riduzione dell’ispessimento al 3° distale esofageo : “… l’esame TC del torace e dell’addome eseguito prima e dopo per fusione e.v. di mdc iodato, con tecnica di acquisizione volumetrica, ha mostrato una complessiva riduzione dell’irregolare ispessimento del tessuto periesofageo al 3° distale, in sede sovra e sottocardiale, con interessamento del fondo gastrico. L’area di interesse mostra subire un evidente enhancement alla perfusione del mdc iodato…”
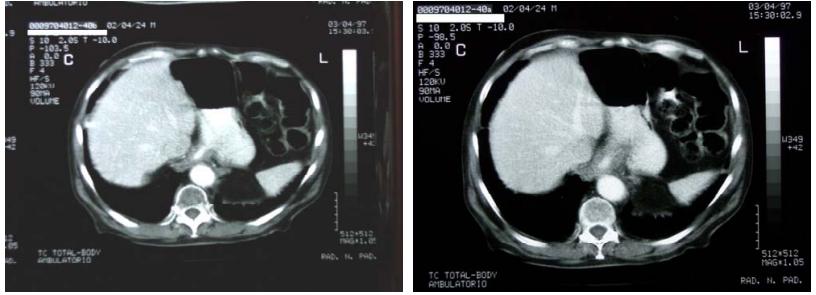
29/10/97— Ricovero ospedaliero per DISFAGIA
Viene eseguita EGDS + biopsia, per valutare eventuale posizionamento di protesi.
REFERTO: Esplorazione endoscopica negativa dell’esofago prossimale. A livello sovracardiale estendentesi fino sotto il cardias in sede fundica si reperta processo infiltrativo con sensibile riduzione del lume esofageo e lesioni necrotiche. Consistenza dura al prelievo bioptico.
L’istologico della biopsia della zona sovracardiale ispessita e sospetta esclude la presenza di cellule neoplastiche.
ISTOLOGICO : Mucosa gastrica con intensa flogosi acuta e cronica e detriti da fondo di ulcerazioni.
20/7/1998—Eseguita TC Total Body di controllo
TC TORACE :
Esame eseguito dopo somministrazione di mdc. Non evidenti alterazioni tomodensitometriche di tipo focale a carico dei parenchimi polmonari. Evidenza di aree disventilatorie in sede basale sn; Non evidenza di linfoadenopatie di rilevanza clinica a carico delle principali stazioni linfonodali mediastiniche. Non versamento pleurico.
TC ADDOME:
Le scansioni eseguite con acquisizione volumetrica a partire dal terzo distale dell’esofago evidenziano un ispessimento parietale del tratto esofageo esaminato, con marcato enhancement delle pareti, non evidenza del lume, contatto con la parete dell’aorta ascendente; non evidenti significative linfoadenopatie loco—regionali
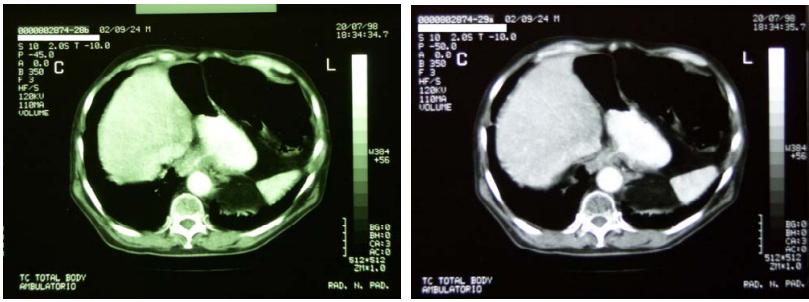
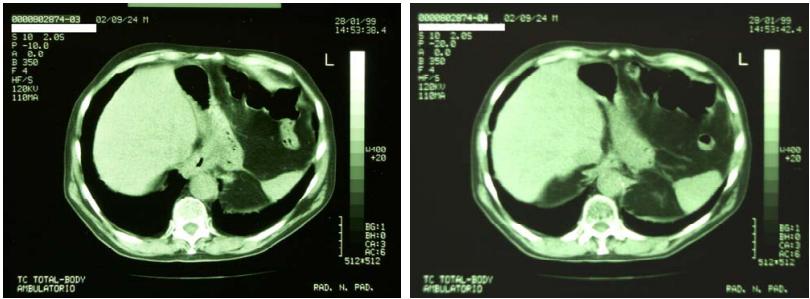
28/1/1999— TC Total Body di controllo
REFERTO : TC TORACE - ADDOME E PELVI:
Non si apprezzano lesioni tomodensitometriche a focolaio. Il sistema ventricolare è in asse non dilatato. Addensamento parenchimale a margini lievemente sfumati in sede basale paracardiaca posteriore dx.
Ispessimento e disomogeneità dell’esofago toracico e trans—diaframmatico con aspetto fortemente sfumato ed irregolare e conseguente riduzione del lume del viscere. Aumento di densità del grasso periviscerale nel tratto sottodiaframmatico. Si apprezzano alcune adenopatie di Ø ai limiti della norma in sede pre e retrocarenale azygotica.
Lo studio del fegato non permette di evidenziare lesioni tomodensitometriche a focolaio in atto. Nulla da segnalare a carico della colecisti. Non significative alterazioni a carico del pancreas, in involuzione adiposa. Non alterazioni a carico della milza.
1/10/2000—Ricovero ospedaliero per episodi di MELENA
Diagnosi: Emorragia acuta e anemia acuta post-emorragica
Eseguita EGDS - REFERTO:
Agevole introduzione dello strumento endoscopico. Negativa esplorazione dell’esofago prossimale.
A livello del 3° distale si osserva restringimento ed ipoelasticità della parete esofagea per tutta la circonferenza senza evidente infiltrazione: si riesce con difficoltà a procedere ed in sede cardiale, sulla parete anteriore, si reperta ampia lesione necrotica di circa 2 cm. già più volte in precedenza descritta che marginalmente, solo in un punto, presenta area di mucosa iperemia con probabili segni di recente sanguinamento. Si esplora il cavo gastrico esente da lesioni.
Iperemia della mucosa duodenale con discreta fragilità da contatto. In tutto il tratto esplorato non si osservano segni di sanguinamento in atto.
Valori EMATOCHIMICI PATOLOGICI:
GR 2260000-2900000;
Hb 6.6 gr% - 9 gr%;
Hti20-28%;
VES 50;
Glicemia 146;
Albuminemia: 2.95 gr/dI.
Viene sottoposto ad emotrasfusioni (6 unità) , sospensione dell’alimentazione orale, terapia con ranitidina e.v.(prima) e con omeprazolo per os (dopo alcuni giorni)
9/10/2000 – Il paziente viene dimesso.
15/11/2001—Ricovero ospedaliero in seguito ad episodio epilettico notturno. Eseguita Tc Cerebrale che “”... Dimostra la presenza di una piccola area di ipodensità localizzata a livello della sostanza bianca adiacente il crocicchio ventricolare di sinistra da riferire ad esiti di lesione su base cerebrovascolare ischemica. Apprezzabile una modesta ipodensità diffusa a livello della sostanza periventricolare come per condizione di sofferenza tissutale su base cerebrovascolare ischemica cronica. Non evidenza di lesioni emorragiche. ”
21/11/2001—il paziente viene dimesso.
28/10/2004—Eseguita TC Total Body di controllo:
TORACE: non evidenti nodulazioni e\o aree di consolidamento polmonari di natura sospetta. Ispessimento pleurico scissurale sx in sede basale con risalita dell'emidiaframma sx. Assenza di versamento pleurico.
Fissità con ispessimento concentrico parietale del terzo distale dell'esofago toracico e della giunzione esofago-gastrica, sostanzialmente immodificato rispetto ai precedenti controlli in visione. Non evidenti tumefazioni linfonodali ilo-mediastinichee sottodiaframmatiche. Fegato di normali dimensioni e morfologia, esente da lesioni focali. Vie biliari non dilatate. Colecisti normodistesa con pareti di normale spessore. Non evidenti alterazioni della milza, del pancreas, dei surreni e del rene dx.
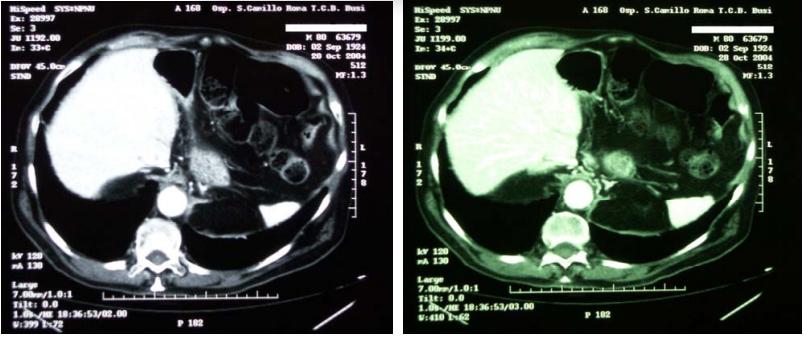
17/1/2007—Eseguita TC Total Body di controllo
REFERTO: TORACE:
Non evidenti alterazioni focali del parenchima polmonare. Non linfoadenopatie ilo-mediastiniche ne' versamento pleurico.
ADDOME E PELVI: Fegato con dimensioni nei limiti, densità parenchimale esente da alterazioni focali. Vie biliari non dilatate, colecisti distesa, alitiasica. Vena porta di calibro regolare e pervia. Surreni con dimensioni e morfologia regolari. Milza nei limiti della norma. Pancreas mal definibile. Reni in sede, rapporto cortico midollare ridotto; cisti renale a sinistra, non ectasia calico pielica. Non evidenti linfoadenopatie interaorto-cavali e lomboaortiche. Vescica simmetricamente distesa con pareti omogenemente ispessite (vescica da sforzo?). Ipertrofia prostatica con disomogenea densità e piccole calcificazioni parenchimali Non linfoadenopatie iliaco-otturatorie.
Il paziente è tuttora vivente e in buone condizioni, si alimenta senza difficoltà.
Attualmente ha ridotto la terapia iniziale ed segue i seguenti trattamenti farmacologici:
Sandostatina Lar 20mg – 1 iniezione intramuscolare ogni 28 gg.
Soluzione di retinoidi – 1 cucchiaio alla mattina a digiuno con
Atiten (vit.D) – 9 gocce assieme ai retinoidi
Melatonina coniugata 2mg – 3 compresse dopo i pasti, ( 9 al dì)
Parlodel 2,5 mg – ¼ di compressa dopo i pasti x 3 volte al dì oltre a:
Luminale - ½ compressa (crisi epilettica)
Enapren 20 – 1 compressa (ipertensione)
Lansox 30 mg – 1 compressa
Plasil 10 – 1 compressa
Venitrin T5 – 1 cerotto
Eutirox 100 – 1 compressa
CONCLUSIONI
La terapia e il decorso clinico.
La chemioradioterapia aveva ottenuto una risposta obiettiva, ma solo parziale, della voluminosa neoplasia esofagea e della estensione periesofagea, oltre che al diaframma, retroperitoneo, stomaco e pancreas, linfonodi regionali ed extraregionali.
Alla ripresa della progressione locale, non potendo proseguire per la grave tossicità con il trattamento chemioradioterapico e nell’impossibilità di un’exeresi chirurgica, il paziente ha chiesto di essere curato con il Metodo Di Bella, che prevede l’impiego sinergico di molecole ad azione differenziante, citostatica, apoptotica, antiproliferativa,antiangiogenica, antimetastatica con il potenziamento dell’ immunita’. La somministrazione continuativa di dosaggi minimi, non citolitici, e pertanto non mutageni, di ciclofosfamide, e grazie all’azione mieloprotettiva, antidegenerativa e trofica su parenchimi e tessuti, della MLT e degli alti dosaggi di Vitamina E, Retinoidi, vitamine C e D3, ha evitato la tossicità midollare, epatorenale, metabolica, cardiocircolatoria, neurologica e la depressione immunitaria, consentendo un graduale recupero e mantenimento di un buon performance status.
I 100 milligrammi giornalieri x os continuativi per oltre 1 anno di ciclofosfamide non hanno pertanto provocato sensibili alterazioni della crasi ematica e della dinamica midollare.
Il paziente ha condotto a domicilio la terapia con una qualità di vita che gli ha consentito di riprendere gradualmente l’attività lavorativa malgrado l’età avanzata .
Farmaci somministrati [componenti della terapia prescritta (MDB)] :
1) Somatostatina (14 aminoacidi) 3 mg iniettati sottocute di notte nell’arco di 10 ore mediante un temporizzatore per la breve emivita ( circa 3 minuti) in coincidenza del picco notturno di increzione del GH;
2) Octreotide, analogo della somatostatina (otto aminoacidi) in formulazione ritardata 20 mg intramuscolo ogni 25 giorni, per una completa saturazione, sia recettoriale che temporale, con potenziamento antiproliferativo e proapoptotico antiangiogenico della somatostatina a 14 aminoacidi;
3) Bromocriptina da 2,5 mg, 1\2 compressa mattino e sera per l’inibizione della prolattina, potente e ubiquituario ormone mitogeno;
4) 7g. di soluzione vitaminica (100 mg x Kg di peso corporeo), almeno 15’ prima del pasto, 3 volte al di’ , secondo la formulazione del prof Di Bella:
Beta carotene…………………… gr 2
Axeroftolo palmitato … ……........gr 1
Ac trans retinoico ( ATRA)…… ..gr 1
Alfatocoferile acetato ………......gr 1000
5) Diidrotachisterolo ( Vit D3 di sintesi) - 10 gocce nello stesso cucchiaio assieme al soluzione vitaminica per ogni somministrazione ( 30 gocce al dì);
6) Melatonina chimicamente complessata con adenosina (mediante un legame di idrogeno) e glicina, secondo la formulazione del Prof Di Bella : Melatonina 12% Adenosina 51% Glicina 37%; compresse da 2 milligrammi , 2 mattino e mezzodì , otto dopo cena
7) Ciclofosfamide compresse 50 mg , una compressa 2 volte al di’;
8) Calcio 1 grammo 2 volte al dì in un bicchiere d’acqua ;
9) Ac ascorbico 2 grammi, insieme al calcio nello stesso bicchiere d’acqua x 2 volte al dì durante il pasto;
10) Glucosamina solfato 500 mg x 3 volte al dì
11) Galattosamina solfato 500 mg x 3 volte al dì
Alla ripresa della progressione locale, non potendo proseguire per la grave tossicità con il trattamento chemioradioterapico e nell’impossibilità di un’exeresi chirurgica, il paziente ha chiesto di essere curato con il Metodo Di Bella, che prevede l’impiego sinergico di molecole ad azione differenziante, citostatica, apoptotica, antiproliferativa,antiangiogenica, antimetastatica con il potenziamento dell’ immunita’. La somministrazione continuativa di dosaggi minimi, non citolitici, e pertanto non mutageni, di ciclofosfamide, e grazie all’azione mieloprotettiva, antidegenerativa e trofica su parenchimi e tessuti, della MLT e degli alti dosaggi di Vitamina E, Retinoidi, vitamine C e D3, ha evitato la tossicità midollare, epatorenale, metabolica, cardiocircolatoria, neurologica e la depressione immunitaria, consentendo un graduale recupero e mantenimento di un buon performance status.
I 100 milligrammi giornalieri x os continuativi per oltre 1 anno di ciclofosfamide non hanno pertanto provocato sensibili alterazioni della crasi ematica e della dinamica midollare.
Il paziente ha condotto a domicilio la terapia con una qualità di vita che gli ha consentito di riprendere gradualmente l’attività lavorativa malgrado l’età avanzata .
Farmaci somministrati [componenti della terapia prescritta (MDB)] :
1) Somatostatina (14 aminoacidi) 3 mg iniettati sottocute di notte nell’arco di 10 ore mediante un temporizzatore per la breve emivita ( circa 3 minuti) in coincidenza del picco notturno di increzione del GH;
2) Octreotide, analogo della somatostatina (otto aminoacidi) in formulazione ritardata 20 mg intramuscolo ogni 25 giorni, per una completa saturazione, sia recettoriale che temporale, con potenziamento antiproliferativo e proapoptotico antiangiogenico della somatostatina a 14 aminoacidi;
3) Bromocriptina da 2,5 mg, 1\2 compressa mattino e sera per l’inibizione della prolattina, potente e ubiquituario ormone mitogeno;
4) 7g. di soluzione vitaminica (100 mg x Kg di peso corporeo), almeno 15’ prima del pasto, 3 volte al di’ , secondo la formulazione del prof Di Bella:
Beta carotene…………………… gr 2
Axeroftolo palmitato … ……........gr 1
Ac trans retinoico ( ATRA)…… ..gr 1
Alfatocoferile acetato ………......gr 1000
5) Diidrotachisterolo ( Vit D3 di sintesi) - 10 gocce nello stesso cucchiaio assieme al soluzione vitaminica per ogni somministrazione ( 30 gocce al dì);
6) Melatonina chimicamente complessata con adenosina (mediante un legame di idrogeno) e glicina, secondo la formulazione del Prof Di Bella : Melatonina 12% Adenosina 51% Glicina 37%; compresse da 2 milligrammi , 2 mattino e mezzodì , otto dopo cena
7) Ciclofosfamide compresse 50 mg , una compressa 2 volte al di’;
8) Calcio 1 grammo 2 volte al dì in un bicchiere d’acqua ;
9) Ac ascorbico 2 grammi, insieme al calcio nello stesso bicchiere d’acqua x 2 volte al dì durante il pasto;
10) Glucosamina solfato 500 mg x 3 volte al dì
11) Galattosamina solfato 500 mg x 3 volte al dì
DISCUSSIONE
La terapia biologica neuro-immuno-endocrina del Prof Luigi Di Bella (MDB) ha lentamente e progressivamente ottenuto una risposta obiettiva completa, in assenza di tossicità, attraverso un meccanismo d’azione recettoriale, differenziante, apoptotico e antiproliferativo, antiangiogenico con criteri, finalità e meccanismi d’azione totalmente difformi dalle consuete terapie citotossiche e citolitiche, dimostrando di potersi sostituire all’intervento chirurgico, alla radioterapia, e alla chemioterapia che notoriamente non ha alcun potere di eradicare i tumori solidi. In questo caso, per l’estesa diffusione neoplastica extraesofagea con voluminose adenopatie disseminate in ambito mediastinico ed addominale, e l’estensione periesofagea, oltre che al diaframma, retroperitoneo , stomaco e pancreas, era stata esclusa una soluzione chirurgica. La risposta obiettiva al MDB (Metodo Di Bella) si è estesa alla risoluzione completa della lesione esofagea e delle sue diramazioni.
RAZIONALE DELLA TERAPIA
La perdita di differenziazione e la proliferazione, anche se in misura diversa, sono denominatori comuni di tutte le neoplasie.
L’espressione recettoriale ubiquitaria della Prolattina [7, 21], e del GH [10, 35], rappresenta una delle conferme del ruolo mitogeno diretto e generalizzato di queste molecole. La proliferazione cellulare è strettamente dipendente dalla Prolattina, dal GH, massimo fattore di crescita, e da molecole mitogene GH dipendenti, da esso positivamente regolate, come EGF, FGF, HGF, IGF1-2, NGF, PDGF, VEGF, TGF, oltre che da fattori di crescita prodotti dall’apparato gastrointestinale, come VIP, CCK, PG. Sia la proliferazione cellulare fisiologica che neoplastica, avvengono per mezzo di queste stesse molecole, che la cellula neoplastica utilizza in misura esponenziale rispetto a quella sana.
Antidoti biologici del GH, come Somatostatina e analoghi, non riducono solo l’espressione e la trascrizione di fattori di crescita altamente mitogeni, come IGF1-2 [9,28,61], EGF [64], FGF [47], ma estendono la loro regolazione negativa ai rispettivi recettori con evidenti riflessi antiproliferativi, e antiangiogenici [1, 4, 17, 25].
E’ noto come l’asse GH-IGF1 abbia una determinante influenza sullo sviluppo biologico neoplastico.
Gli IGFR rispondono mitogenicamente a IGF. L’effetto soppressivo della SST e analoghi sui livelli sierici di IGF1, è sia diretto, attraverso l’inibizione del gene di IGF, che indiretto, mediante la soppressione del GH e pertanto della sua induzione epatica di IGF1. Momenti essenziali dell’angiogenesi, passaggio essenziale della progressione neoplastica, come la cascata dei monociti [73], l’interleukina 8, fattori di crescita essenziali e sinergici per lo sviluppo dell’angiogenesi, come il VEGF, TGF, IGF1, FGF, HGF, PDGF, sono negativamente regolati da Somatostatina e analoghi [1, 4, 9, 14, 25, 68, 69, 72].
L’inibizione dell’angiogenesi indotta dalla SST è sinergicamente potenziata da MLT [11, 12, 36], Retinoidi [31,42,45], vitamina D3 [32,44], Vitamina E [52,63,65] Vitamina C [8,19,51], inibitori prolattinici [68], componenti della matrice extracellulare [37,57] . Ugualmente l’effetto citostatico, antiproliferativo, antimetastatico della Somatostatina è efficacemente sinergizzato dagli altri componenti del MDB: Retinoidi [56,58] MLT [33,41] Vit D3 [5,24] Cabergolina e Bromocriptina ( inibitori prolattinici) [17,7] Glucosamina solfato, condroitinsolfato solfato, componenti della matrice extracellulare [6,59] Vit E [22,43,52,63,67] Vit C [8,19,51] È stato dimostrato il rapporto causale tra espressione recettoriale del GH e induzione e progressione tumorale, rilevando istochimicamente concentrazioni di GHR nettamente superiori nei tessuti tumorali, rispetto ai fisiologici, evidenziando il potente ruolo mitogeno del GH con indice proliferativo dose dipendente[35]. Esso è sia diretto, recettoriale, che indiretto, attraverso l’induzione dell’espressione epatica di IGF1, GH dipendente.
L’asse GH-IGF1 ha un ruolo determinante sul comportamento biologico di molte neoplasie. In un’elevatissima e subtotale percentuale di varietà di cellule neoplastiche sono stati individuati recettori IGF1, che rispondono mitogenicamente al ligando.
La Somatostatina esercita l’attività antiblastica sia direttamente, attraverso l’inibizione dell’espressione del gene IGF1, che indirettamente, mediante la soppressione del GH, da cui dipende l’increzione di IGF1 [61]. Ampiamente documentata è anche l’attività inibitoria della SST su un altro potente fattore di crescita mitogeno, EGF, attraverso molteplici meccanismi: - inibizione dose dipendente della fosforilazione tirosinica indotta dall’attivazione di EGFR da parte di EGF [49]; - riduzione di EGFR nelle cellule tumorali [64]; - riduzione dell’espressione di EGF [22]; - abbattimento della concentrazione plasmatica di EGF [9]. Mitogeni prodotti dall’apparato gastrointestinale, come VIP, CCK, PG, sono potentemente inibiti dalla somatostatina e/o octreotide [28], la cui efficacia è potenziata attraverso un meccanismo sinergico fattoriale con gli altri componenti del MDB. La letteratura ha pertanto confermato i meccanismi d’azione antineoplastici differenzianti e antiproliferativi, antiangiogenetici e antimetastatici di tutti i componenti del MDB.
In questo caso gli esami ematochimici non hanno evidenziato danni, o tossicità, indotti dal MDB. Il risultato obiettivo, in assenza di tossicità, mediante la riduzione lenta e progressiva fino alla scomparsa delle estese lesioni neoplastiche iniziali, delle adenopatie, insieme al blocco di ogni progressione loco regionale o disseminazione metastatica, evidenzia l’efficacia di questa multiterapia ed è conforme ai positivi risultati già pubblicati sull’uso di questo metodo nei LNH a basso grado e carcinomi polmonari al 3° e 4° stadio.
Il MDB, senza necessità di ricovero ospedaliero e neppure di day hospital, in assenza di tossicità ha recuperato la funzionalità esofagea, il trofismo e funzionalità di organi e tessuti, consentendo, a distanza di tredici anni, una qualità di vita fisiologica e attiva, fino all’età di 84 anni.
Si può ragionevolmente ipotizzare pertanto che l’applicazione precoce, e come terapia di prima linea di questo metodo, in un organismo non debilitato dagli effetti tossici, mutageni e immunodepressivi della chemio-radioterapia, potrebbe conseguire risultati decisamente più rapidi.
Riteniamo utile segnalare il caso per invitare ad un maggiore interesse, studio e approfondimento sulle possibilità aperte in oncologia dalla terapia immunoneuroendocrina, biologica e recettoriale MDB.
REFERENZE
1. Albini A, Florio T, Giunciuglio D, et al. Somatostatin controls Kaposi's sarcoma tumor growth through inhibition of angiogenesis. FASEB J. 1999; 13(6): 647-655.
2. Ashino H, Shimamura M, Nakajima H, , et al. Novel function of ascorbic acid as an angiostatic factor. Angiogenesis. 2003; 6(4): 259-269.
3. Barnett P. Somatostatin and somatostatin receptor physiology. Endocrine. 2003; 20(3): 255-264
4. Barrie R, Woltering EA, Hajarizadeh H,. Inhibition of angiogenesis by somatostatin and somatostatin-like compounds is structurally dependent. J Surg Res. 1993; 55(4): 446-450.
5. Barroga EF, Kadosawa T, Okumura M,. Inhibitory effects of 22-oxa-calcitriol and all- trans retinoic acid on the growth of a canine osteosarcoma derived cell-line in vivo and its pulmonary metastasis in vivo. Res Vet Sci. 2000; 68(1): 79-87.
6. Batra RK, Olsen JC, Hoganson DK, Retroviral gene transfer is inhibited by chondroitin sulfate proteoglycans/glycosaminoglycans in malignant pleural effusions. J Biol Chem. 1997; 272(18): 11736-43.
7. Ben-Jonathan N, Liby K, McFarland M, Prolactin as an autocrine/paracrine growth factor in human cancer. Trends Endocrinol Metab. 2002; 13(6):245-250.
8. Cameron E, Pauling L, Leibovitz B. Ascorbic acid and cancer: a review. Cancer Res. 1979; 39(3): 663-681.
9. Cascinu S, Del Ferro E, Ligi M, Staccioli, et al. Inhibition of vascular endothelial growth factor by octreotide in colorectal cancer patients. Cancer Invest. 2001; 19(1): 8-12.
10. De Souza I, Morgan L, Lewis UL,. Growth-hormone dependence among human breast cancers. Lancet. 1974; 2(7874):182-184.
11. Di Bella L, Gualano L. Key aspects of melatonin physiology: thirty years of research. Neuro Endocrinol Lett. 2006; 27(4): 425-432.
12. Di Bella L, Rossi MT, Scalera G. Perspectives in pineal functions. Prog Brain Res. 1979; 52: 475-478.
13. Dong LM, Kristal AR, Peters U, Dietary supplement use and risk of neoplastic progression in esophageal adenocarcinoma: a prospective study.Nutr Cancer. 2008 Jan-Feb;60(1):39-48
14. Florio T, Morini M, Villa V, et al. Somatostatin inhibits tumor angiogenesis and growth via somatostatin receptor-3-mediated regulation of endothelial nitric oxide synthase and mitogenactivated protein kinase activities. Endocrinology. 2003; 144(4): 1574-1584.
15. Giovannucci E, Liu Y, Willett WC.Cancer incidence and mortality and vitamin D in black and white male health professionals.Cancer Epidemiol Biomarkers Prev. 2006 Dec;15(12):2467-72. Epub 2006 Nov 28.
16. Griffin M, Sweeney EC.The relationship of endocrine cells, dysplasia and carcinoembryonic antigen in Barrett's mucosa to adenocarcinoma of the oesophagus.Histopathology. 1987 Jan;11(1):53-62.
17. Gruszka A, Pawlikowski M, Kunert-Radek J. Anti-tumoral action of octreotide and bromocriptine on the experimental rat prolactinoma: anti-proliferative and pro-apoptotic effects. Neuro Endocrinol Lett. 2001; 22(5): 343-348.
18. Hashimoto Y, Shimada Y, Itami A, Growth inhibition through activation of peroxisome proliferator-activated receptor gamma in human oesophageal squamous cell carcinoma.Eur J Cancer. 2003 Oct;39(15):2239-46
19. Head KA. Ascorbic acid in the prevention and treatment of cancer. Altern Med Rev. 1998; 3(3): 174-186.
20. Held-Feindt J, Krisch B, Mentlein R. Molecular analysis of the somatostatin receptor subtype 2 in human glioma cells. Brain Res Mol Brain Res. 1999; 64(1): 101-7.
21. Hooghe R, Merchav S, Gaidano G, A role for growth hormone and prolactin in leukaemia and lymphoma? Cell Mol Life Sci. 1998; 54(10): 1095-1101.
22. Israel K, Yu W, Sanders BG, Kline K. Vitamin E succinate induces apoptosis in human prostate cancer cells: role for Fas in vitamin E succinate-triggered apoptosis. Nutr Cancer. 2000; 36(1): 90-100.
23. Jatoi A, Thomas CR Jr Esophageal cancer and the esophagus: challenges and potential strategies for selective cytoprotection of the tumor-bearing organ during cancer treatment. Semin Radiat Oncol. 2002 Jan;12(1 Suppl 1):62-7.
24. Jensen SS, Madsen MW, Lukas J, Binderup L, Bartek J. Inhibitory effects of 1alpha,25dihydroxyvitamin D(3) on the G(1)-S phase-controlling machinery. Mol Endocrinol. 2001; 15(8): 1370-1380.
25. Jia WD , Xu GL , Xu RN, et al. Octreotide acts as an antitumor angiogenesis compound and suppresses tumor growth in nude mice bearing human hepatocellular carcinoma xenografts. J Cancer Res Clin Oncol. 2003; 129(6): 327-334.
26. Jin Z, Mori Y, Hamilton JP, Hypermethylation of the somatostatin promoter is a common, early event in human esophageal carcinogenesis. Cancer. 2008 Jan 1;112(1):43-9.
27. Kapil U, Srivastav M, Nayar D. Vitamin 'A' and oesophageal cancer. Trop Gastroenterol. 1993 Jul-Sep;14(3):87-90.
28. Kath R, Höffken K. The significance of somatostatin analogues in the antiproliferative treatment of carcinomas. Recent Results Cancer Res. 2000; 153: 23-43.
29. Khuri FR, Kim ES, Lee JJ . The impact of smoking status, disease stage, and index tumor site on second primary tumor incidence and tumor recurrence in the head and neck retinoid chemoprevention trial. Cancer Epidemiol Biomarkers Prev. 2001 Aug;10(8):823-9.
30. Kidd PM. The use of mushroom glucans and proteoglycans in cancer treatment.Altern Med Rev. 2000 Feb;5(1):4-27. Review.
31. Kini AR, Peterson LA, Tallman MS, Lingen MW. Angiogenesis in acute promyelocytic leukemia: induction by vascular endothelial growth factor and inhibition by all-trans retinoic acid. Blood. 2001; 97(12): 3919-3924
32. Kisker O, Onizuka S, Becker CM, Fannon M, Flynn E, D'Amato R, et al. Vitamin D binding protein-macrophage activating factor (DBP-maf) inhibits angiogenesis and tumor growth in mice. Neoplasia. 2003; 5(1): 32-40.
33. Kvetnoĭ IM, Levin IM. Melatonin and tumor growth.(In Russian with English abstract). Eksp Onkol. 1986; 8(4): 11-15.
34. Launoy G, Milan C, Day NE, Pienkowski MP,.Diet and squamous-cell cancer of the oesophagus: a French multicentre case-control study.Int J Cancer. 1998 Mar 30;76(1):7-12.
35. Lincoln DT, Sinowatz F, Temmim-Baker L, et al. Growth hormone receptor expression in the nucleus and cytoplasm of normal and neoplastic cells. Histochem Cell Biol. 1998; 109(2): 141-159
36. Lissoni P, Rovelli F, Malugani F, Bucovec R, Conti A, Maestroni GJ. Anti-angiogenic activity of melatonin in advanced cancer patients. Neuro Endocrinol Lett. 2001; 22(1): 45-47.
37. Liu G, Wu M, Levi G, Inhibition of cancer cell growth by all-trans retinoic acid and its analog N-(4-hydroxyphenyl) retinamide: a possible mechanism of action via regulation of retinoid receptors expression. Int J Cancer. 1998 Oct 5;78(2):248-54
38. Liu Y, Yang H, Otaka K, Takatsuki H, Sakanishi A. Effects of vascular endothelial growth
factor (VEGF) and chondroitin sulfate A on human monocytic THP-1 cell migration. Colloids Surf B Biointerfaces. 2005; 43(3-4): 216-220.
39. Lotan R. Retinoids and chemoprevention of aerodigestive tract cancers Cancer Metastasis Rev. 1997 Sep-Dec;16(3-4):349-56.
40. Lubin JH, Virtamo J, Weinstein SJ.Cigarette smoking and cancer: intensity patterns in the alpha-tocopherol, beta-carotene cancer prevention study in Finnish men.Am J Epidemiol. 2008 Apr 15;167(8):970-5. Epub 2008 Feb 3.
41. Maestroni GJ, Hertens E, Galli P, Conti A, Pedrinis E. Melatonin-induced T-helper cell hematopoietic cytokines resembling both interleukin-4 and dynorphin. J Pineal Res. 1996; 21(3): 131-9.
42. Majewski S, Szmurlo A, Marczak M, Jablonska S, Bollag W. Synergistic effect of retinoids and interferon alpha on tumor-induced angiogenesis: anti-angiogenic effect on HPV-harboring tumor-cell lines. Int J Cancer. 1994; 57(1): 81-85.
43. Malafa MP, Fokum FD, Smith L, Louis A. Inhibition of angiogenesis and promotion of melanoma dormancy by vitamin E succinate. Ann Surg Oncol. 2002; 9(10): 1023-1032.
44. Mantell DJ, Owens PE, Bundred NJ, Mawer EB, Canfield AE. 1 alpha,25-dihydroxyvitamin D(3) inhibits angiogenesis in vitro and in vivo. Circ Res. 2000; 87(3): 214-220.
45. McMillan K, Perepelitsyn I, Wang Z, Shapshay SM. Tumor growth inhibition and regression induced by photothermal vascular targeting and angiogenesis inhibitor retinoic acid. Cancer Lett. 1999; 137(1): 35-44.
46. Meggouh F, Lointier P, Pezet D, Evidence of 1,25-dihydroxyvitamin D3-receptors in human digestive mucosa and carcinoma tissue biopsies taken at different levels of the digestive tract, in 152 patients.J Steroid Biochem 1990 Jun;36 (1-2): 143-7
47. Mentlein R, Eichler O, Forstreuter F, Held-Feindt J. Somatostatin inhibits the production of vascular endothelial growth factor in human glioma cells. Int J Cancer. 2001; 92(4): 545-550.
48. Mikami S, Ohashi K, Usui Y, Nemoto T, Katsube K, Yanagishita M, Nakajima M, Nakamura K, Koike M. Loss of syndecan-1 and increased expression of heparanase in invasive esophageal carcinomas Jpn J Cancer Res. 2001 Oct;92(10):1062-73
9. Mishima M, Yano T, Jimbo H, Yano N, Morita Y, Yoshikawa H, et al. Inhibition of human endometrial cancer cell growth in vitro and in vivo by somatostatin analog RC-160. Am J Obstet Gynecol. 1999; 181(3): 583-590.
50. Muller A, Nakagawa H, Rustgi AK. Retinoic acid and N-(4-hydroxy-phenyl) retinamide suppress growth of esophageal squamous carcinoma cell lines. Cancer Lett. 1997 Feb 26;113(1-2):95-101
51. Murata A, Morishige F, Yamaguchi H. Prolongation of survival times of terminal cancer patients by administration of large doses of ascorbate. Int J Vitam Nutr Res Suppl. 1982; 23: 103-113.
52. Neuzil J, Kagedal K, Andera L, Weber C, Brunk UT. Vitamin E analogs: a new class of multiple action agents with anti-neoplastic and anti-atherogenic activity. Apoptosis. 2002; 7(2): 179-87.
53. Norsa A. and Martino V.. Somatostatin, Retinoidi, Melatonin, Vitamin D, Bromocriptine, and Cyclophosphamide in Chemotherapy-Pretreated Patients with Advanced Lung Adenocarcinoma and Low Performance Status. Cancer Biotherapy & Radiopharmaceuticals Volume 22, Number 1, 2007
54. Odeleye OE, Eskelson CD, Mufti SI, Watson RR Vitamin E inhibition of lipid peroxidation and ethanol-mediated promotion of esophageal tumorigenesis. Nutr Cancer. 1992;17(3):223-34
55. Odeleye OE, Eskelson CD, Mufti SI, Watson RR.Vitamin E protection against nitrosamine induced esophageal tumor incidence in mice immunocompromised by retroviral infection. Carcinogenesis. 1992 Oct;13(10):1811-6.
56. Onogi N, Okuno M, Matsushima-Nishiwaki R, Fukutomi Y, Moriwaki H, Muto Y, et al. Antiproliferative effect of carotenoids on human colon cancer cells without conversion to retinoic acid. Nutr Cancer. 1998; 32(1): 20-24.
57. Ozerdem U, Stallcup WB. Pathological angiogenesis is reduced by targeting pericytes via the NG2 proteoglycan. Angiogenesis. 2004; 7(3): 269-276.
58. Piedrafita FJ, Pfahl M. Retinoid-induced apoptosis and Sp1 cleavage occur independently of transcription and require caspase activation. Mol Cell Biol. 1997; 17(11): 6348-58.
59. Pumphrey CY, Theus AM, Li S, Parrish RS, Sanderson RD. Neoglycans, carbodiimide-modified glycosaminoglycans: a new class of anticancer agents that inhibit cancer cell proliferation and induce apoptosis. Cancer Res. 2002; 62(13): 3722-8.
60. Roth AD, Morant R, Alberto P High dose etretinate and interferon-alpha--a phase I study in squamous cell carcinomas and transitional cell carcinomas. Acta Oncol. 1999;38(5):613-7
61. Schally AV, Comaru-Schally AM, Nagy A, Kovacs M, Szepeshazi K, Plonowski A, et al. Hypothalamic hormones and cancer. Front Neuroendocrinol. 2001; 22(4): 248-291.
62. Shimizu M, Suzui M, Deguchi A,. Effects of acyclic retinoid on growth, cell cycle control, epidermal growth factor receptor signaling, and gene expression in human squamous cell carcinoma cells. Clin Cancer Res. 2004 Feb 1;10(3):1130-40
63. Shklar G, Schwartz JL. Vitamin E inhibits experimental carcinogenesis and tumour angiogenesis. Eur J Cancer B Oral Oncol. 1996; 32B(2): 114-119.
64. Szepesházi K, Halmos G, Schally AV, Arencibia JM, Groot K, Vadillo-Buenfil M, et al. Growth
inhibition of experimental pancreatic cancers and sustained reduction in epidermal growth factor receptors during therapy with
65. Tang FY, Meydani M. Green tea catechins and vitamin E inhibit angiogenesis of human microvascular endothelial cells through suppression of IL-8 production. Nutr Cancer. 2001; 41(1-2): 119-125.
66. Todisco M., MD, Piergiorgio Casaccia, MD e Nazzareno Rossi, ASL 13 in Sondrio e ASL 106 in Teramo. Ciclofosfamide piu’ somatostatina, bromocriptina, retinoidi, melatonina e ACTH nel trattamento dei linfomi non –Hodgkin di basso grado in stadio avanzato: risultati di una
sperimentazione di fase 2. Cancer Biotherapy & Radiopharmaceuticals Volume 16, Number 2, 2001 Mary Ann Liebert, Inc.
67. Turley JM, Funakoshi S, Ruscetti FW, Kasper J, Murphy WJ, Longo DL, et al. Growth inhibition and apoptosis of RL human B lymphoma cells by vitamin E succinate and retinoic acid: role for transforming growth factor beta. Cell Growth Differ. 1995; 6(6): 655-663.
68. Turner HE, Nagy Z, Gatter KC, Esiri MM, Harris AL, Wass JA. Angiogenesis in pituitary adenomas - relationship to endocrine function, treatment and outcome. J Endocrinol. 2000; 165(2): 475-481.
69. Vidal S, Oliveira MC, Kovacs K, Scheithauer BW, Lloyd R. Immunolocalization of vascular endothelial growth factor in the GH3 cell line. Cell Tissue Res. 2000; 300(1): 83-88.
70. Wang C, Tammi M, Guo H, Tammi R.Hyaluronan. Distribution in the normal epithelium of esophagus, stomach, and colon and their cancers.Am J Pathol. 1996 Jun;148(6):1861-9.
71. Wang ZH, Yam HF, Or PC, Yang L . Effects of all-trans-retinoic acid on human esophageal carcinoma cells and their nuclear matrices. Anticancer Res. 1999 Jan-Feb;19(1A):563-8
72. Watson JC, Balster DA, Gebhardt BM, O'Dorisio TM, O'Dorisio MS, Espenan GD, et al. Growing vascular endothelial cells express somatostatin subtype 2 receptors. Br J Cancer. 2001; 85(2): 266-272.
73. Wiedermann CJ, Reinisch N, Braunsteiner H. Stimulation of monocyte chemotaxis by human growth hormone and its deactivation by somatostatin. BZou XN, Taylor PR, Mark SD, lood. 1993; 82(3): 954-960.
2. Ashino H, Shimamura M, Nakajima H, , et al. Novel function of ascorbic acid as an angiostatic factor. Angiogenesis. 2003; 6(4): 259-269.
3. Barnett P. Somatostatin and somatostatin receptor physiology. Endocrine. 2003; 20(3): 255-264
4. Barrie R, Woltering EA, Hajarizadeh H,. Inhibition of angiogenesis by somatostatin and somatostatin-like compounds is structurally dependent. J Surg Res. 1993; 55(4): 446-450.
5. Barroga EF, Kadosawa T, Okumura M,. Inhibitory effects of 22-oxa-calcitriol and all- trans retinoic acid on the growth of a canine osteosarcoma derived cell-line in vivo and its pulmonary metastasis in vivo. Res Vet Sci. 2000; 68(1): 79-87.
6. Batra RK, Olsen JC, Hoganson DK, Retroviral gene transfer is inhibited by chondroitin sulfate proteoglycans/glycosaminoglycans in malignant pleural effusions. J Biol Chem. 1997; 272(18): 11736-43.
7. Ben-Jonathan N, Liby K, McFarland M, Prolactin as an autocrine/paracrine growth factor in human cancer. Trends Endocrinol Metab. 2002; 13(6):245-250.
8. Cameron E, Pauling L, Leibovitz B. Ascorbic acid and cancer: a review. Cancer Res. 1979; 39(3): 663-681.
9. Cascinu S, Del Ferro E, Ligi M, Staccioli, et al. Inhibition of vascular endothelial growth factor by octreotide in colorectal cancer patients. Cancer Invest. 2001; 19(1): 8-12.
10. De Souza I, Morgan L, Lewis UL,. Growth-hormone dependence among human breast cancers. Lancet. 1974; 2(7874):182-184.
11. Di Bella L, Gualano L. Key aspects of melatonin physiology: thirty years of research. Neuro Endocrinol Lett. 2006; 27(4): 425-432.
12. Di Bella L, Rossi MT, Scalera G. Perspectives in pineal functions. Prog Brain Res. 1979; 52: 475-478.
13. Dong LM, Kristal AR, Peters U, Dietary supplement use and risk of neoplastic progression in esophageal adenocarcinoma: a prospective study.Nutr Cancer. 2008 Jan-Feb;60(1):39-48
14. Florio T, Morini M, Villa V, et al. Somatostatin inhibits tumor angiogenesis and growth via somatostatin receptor-3-mediated regulation of endothelial nitric oxide synthase and mitogenactivated protein kinase activities. Endocrinology. 2003; 144(4): 1574-1584.
15. Giovannucci E, Liu Y, Willett WC.Cancer incidence and mortality and vitamin D in black and white male health professionals.Cancer Epidemiol Biomarkers Prev. 2006 Dec;15(12):2467-72. Epub 2006 Nov 28.
16. Griffin M, Sweeney EC.The relationship of endocrine cells, dysplasia and carcinoembryonic antigen in Barrett's mucosa to adenocarcinoma of the oesophagus.Histopathology. 1987 Jan;11(1):53-62.
17. Gruszka A, Pawlikowski M, Kunert-Radek J. Anti-tumoral action of octreotide and bromocriptine on the experimental rat prolactinoma: anti-proliferative and pro-apoptotic effects. Neuro Endocrinol Lett. 2001; 22(5): 343-348.
18. Hashimoto Y, Shimada Y, Itami A, Growth inhibition through activation of peroxisome proliferator-activated receptor gamma in human oesophageal squamous cell carcinoma.Eur J Cancer. 2003 Oct;39(15):2239-46
19. Head KA. Ascorbic acid in the prevention and treatment of cancer. Altern Med Rev. 1998; 3(3): 174-186.
20. Held-Feindt J, Krisch B, Mentlein R. Molecular analysis of the somatostatin receptor subtype 2 in human glioma cells. Brain Res Mol Brain Res. 1999; 64(1): 101-7.
21. Hooghe R, Merchav S, Gaidano G, A role for growth hormone and prolactin in leukaemia and lymphoma? Cell Mol Life Sci. 1998; 54(10): 1095-1101.
22. Israel K, Yu W, Sanders BG, Kline K. Vitamin E succinate induces apoptosis in human prostate cancer cells: role for Fas in vitamin E succinate-triggered apoptosis. Nutr Cancer. 2000; 36(1): 90-100.
23. Jatoi A, Thomas CR Jr Esophageal cancer and the esophagus: challenges and potential strategies for selective cytoprotection of the tumor-bearing organ during cancer treatment. Semin Radiat Oncol. 2002 Jan;12(1 Suppl 1):62-7.
24. Jensen SS, Madsen MW, Lukas J, Binderup L, Bartek J. Inhibitory effects of 1alpha,25dihydroxyvitamin D(3) on the G(1)-S phase-controlling machinery. Mol Endocrinol. 2001; 15(8): 1370-1380.
25. Jia WD , Xu GL , Xu RN, et al. Octreotide acts as an antitumor angiogenesis compound and suppresses tumor growth in nude mice bearing human hepatocellular carcinoma xenografts. J Cancer Res Clin Oncol. 2003; 129(6): 327-334.
26. Jin Z, Mori Y, Hamilton JP, Hypermethylation of the somatostatin promoter is a common, early event in human esophageal carcinogenesis. Cancer. 2008 Jan 1;112(1):43-9.
27. Kapil U, Srivastav M, Nayar D. Vitamin 'A' and oesophageal cancer. Trop Gastroenterol. 1993 Jul-Sep;14(3):87-90.
28. Kath R, Höffken K. The significance of somatostatin analogues in the antiproliferative treatment of carcinomas. Recent Results Cancer Res. 2000; 153: 23-43.
29. Khuri FR, Kim ES, Lee JJ . The impact of smoking status, disease stage, and index tumor site on second primary tumor incidence and tumor recurrence in the head and neck retinoid chemoprevention trial. Cancer Epidemiol Biomarkers Prev. 2001 Aug;10(8):823-9.
30. Kidd PM. The use of mushroom glucans and proteoglycans in cancer treatment.Altern Med Rev. 2000 Feb;5(1):4-27. Review.
31. Kini AR, Peterson LA, Tallman MS, Lingen MW. Angiogenesis in acute promyelocytic leukemia: induction by vascular endothelial growth factor and inhibition by all-trans retinoic acid. Blood. 2001; 97(12): 3919-3924
32. Kisker O, Onizuka S, Becker CM, Fannon M, Flynn E, D'Amato R, et al. Vitamin D binding protein-macrophage activating factor (DBP-maf) inhibits angiogenesis and tumor growth in mice. Neoplasia. 2003; 5(1): 32-40.
33. Kvetnoĭ IM, Levin IM. Melatonin and tumor growth.(In Russian with English abstract). Eksp Onkol. 1986; 8(4): 11-15.
34. Launoy G, Milan C, Day NE, Pienkowski MP,.Diet and squamous-cell cancer of the oesophagus: a French multicentre case-control study.Int J Cancer. 1998 Mar 30;76(1):7-12.
35. Lincoln DT, Sinowatz F, Temmim-Baker L, et al. Growth hormone receptor expression in the nucleus and cytoplasm of normal and neoplastic cells. Histochem Cell Biol. 1998; 109(2): 141-159
36. Lissoni P, Rovelli F, Malugani F, Bucovec R, Conti A, Maestroni GJ. Anti-angiogenic activity of melatonin in advanced cancer patients. Neuro Endocrinol Lett. 2001; 22(1): 45-47.
37. Liu G, Wu M, Levi G, Inhibition of cancer cell growth by all-trans retinoic acid and its analog N-(4-hydroxyphenyl) retinamide: a possible mechanism of action via regulation of retinoid receptors expression. Int J Cancer. 1998 Oct 5;78(2):248-54
38. Liu Y, Yang H, Otaka K, Takatsuki H, Sakanishi A. Effects of vascular endothelial growth
factor (VEGF) and chondroitin sulfate A on human monocytic THP-1 cell migration. Colloids Surf B Biointerfaces. 2005; 43(3-4): 216-220.
39. Lotan R. Retinoids and chemoprevention of aerodigestive tract cancers Cancer Metastasis Rev. 1997 Sep-Dec;16(3-4):349-56.
40. Lubin JH, Virtamo J, Weinstein SJ.Cigarette smoking and cancer: intensity patterns in the alpha-tocopherol, beta-carotene cancer prevention study in Finnish men.Am J Epidemiol. 2008 Apr 15;167(8):970-5. Epub 2008 Feb 3.
41. Maestroni GJ, Hertens E, Galli P, Conti A, Pedrinis E. Melatonin-induced T-helper cell hematopoietic cytokines resembling both interleukin-4 and dynorphin. J Pineal Res. 1996; 21(3): 131-9.
42. Majewski S, Szmurlo A, Marczak M, Jablonska S, Bollag W. Synergistic effect of retinoids and interferon alpha on tumor-induced angiogenesis: anti-angiogenic effect on HPV-harboring tumor-cell lines. Int J Cancer. 1994; 57(1): 81-85.
43. Malafa MP, Fokum FD, Smith L, Louis A. Inhibition of angiogenesis and promotion of melanoma dormancy by vitamin E succinate. Ann Surg Oncol. 2002; 9(10): 1023-1032.
44. Mantell DJ, Owens PE, Bundred NJ, Mawer EB, Canfield AE. 1 alpha,25-dihydroxyvitamin D(3) inhibits angiogenesis in vitro and in vivo. Circ Res. 2000; 87(3): 214-220.
45. McMillan K, Perepelitsyn I, Wang Z, Shapshay SM. Tumor growth inhibition and regression induced by photothermal vascular targeting and angiogenesis inhibitor retinoic acid. Cancer Lett. 1999; 137(1): 35-44.
46. Meggouh F, Lointier P, Pezet D, Evidence of 1,25-dihydroxyvitamin D3-receptors in human digestive mucosa and carcinoma tissue biopsies taken at different levels of the digestive tract, in 152 patients.J Steroid Biochem 1990 Jun;36 (1-2): 143-7
47. Mentlein R, Eichler O, Forstreuter F, Held-Feindt J. Somatostatin inhibits the production of vascular endothelial growth factor in human glioma cells. Int J Cancer. 2001; 92(4): 545-550.
48. Mikami S, Ohashi K, Usui Y, Nemoto T, Katsube K, Yanagishita M, Nakajima M, Nakamura K, Koike M. Loss of syndecan-1 and increased expression of heparanase in invasive esophageal carcinomas Jpn J Cancer Res. 2001 Oct;92(10):1062-73
9. Mishima M, Yano T, Jimbo H, Yano N, Morita Y, Yoshikawa H, et al. Inhibition of human endometrial cancer cell growth in vitro and in vivo by somatostatin analog RC-160. Am J Obstet Gynecol. 1999; 181(3): 583-590.
50. Muller A, Nakagawa H, Rustgi AK. Retinoic acid and N-(4-hydroxy-phenyl) retinamide suppress growth of esophageal squamous carcinoma cell lines. Cancer Lett. 1997 Feb 26;113(1-2):95-101
51. Murata A, Morishige F, Yamaguchi H. Prolongation of survival times of terminal cancer patients by administration of large doses of ascorbate. Int J Vitam Nutr Res Suppl. 1982; 23: 103-113.
52. Neuzil J, Kagedal K, Andera L, Weber C, Brunk UT. Vitamin E analogs: a new class of multiple action agents with anti-neoplastic and anti-atherogenic activity. Apoptosis. 2002; 7(2): 179-87.
53. Norsa A. and Martino V.. Somatostatin, Retinoidi, Melatonin, Vitamin D, Bromocriptine, and Cyclophosphamide in Chemotherapy-Pretreated Patients with Advanced Lung Adenocarcinoma and Low Performance Status. Cancer Biotherapy & Radiopharmaceuticals Volume 22, Number 1, 2007
54. Odeleye OE, Eskelson CD, Mufti SI, Watson RR Vitamin E inhibition of lipid peroxidation and ethanol-mediated promotion of esophageal tumorigenesis. Nutr Cancer. 1992;17(3):223-34
55. Odeleye OE, Eskelson CD, Mufti SI, Watson RR.Vitamin E protection against nitrosamine induced esophageal tumor incidence in mice immunocompromised by retroviral infection. Carcinogenesis. 1992 Oct;13(10):1811-6.
56. Onogi N, Okuno M, Matsushima-Nishiwaki R, Fukutomi Y, Moriwaki H, Muto Y, et al. Antiproliferative effect of carotenoids on human colon cancer cells without conversion to retinoic acid. Nutr Cancer. 1998; 32(1): 20-24.
57. Ozerdem U, Stallcup WB. Pathological angiogenesis is reduced by targeting pericytes via the NG2 proteoglycan. Angiogenesis. 2004; 7(3): 269-276.
58. Piedrafita FJ, Pfahl M. Retinoid-induced apoptosis and Sp1 cleavage occur independently of transcription and require caspase activation. Mol Cell Biol. 1997; 17(11): 6348-58.
59. Pumphrey CY, Theus AM, Li S, Parrish RS, Sanderson RD. Neoglycans, carbodiimide-modified glycosaminoglycans: a new class of anticancer agents that inhibit cancer cell proliferation and induce apoptosis. Cancer Res. 2002; 62(13): 3722-8.
60. Roth AD, Morant R, Alberto P High dose etretinate and interferon-alpha--a phase I study in squamous cell carcinomas and transitional cell carcinomas. Acta Oncol. 1999;38(5):613-7
61. Schally AV, Comaru-Schally AM, Nagy A, Kovacs M, Szepeshazi K, Plonowski A, et al. Hypothalamic hormones and cancer. Front Neuroendocrinol. 2001; 22(4): 248-291.
62. Shimizu M, Suzui M, Deguchi A,. Effects of acyclic retinoid on growth, cell cycle control, epidermal growth factor receptor signaling, and gene expression in human squamous cell carcinoma cells. Clin Cancer Res. 2004 Feb 1;10(3):1130-40
63. Shklar G, Schwartz JL. Vitamin E inhibits experimental carcinogenesis and tumour angiogenesis. Eur J Cancer B Oral Oncol. 1996; 32B(2): 114-119.
64. Szepesházi K, Halmos G, Schally AV, Arencibia JM, Groot K, Vadillo-Buenfil M, et al. Growth
inhibition of experimental pancreatic cancers and sustained reduction in epidermal growth factor receptors during therapy with
65. Tang FY, Meydani M. Green tea catechins and vitamin E inhibit angiogenesis of human microvascular endothelial cells through suppression of IL-8 production. Nutr Cancer. 2001; 41(1-2): 119-125.
66. Todisco M., MD, Piergiorgio Casaccia, MD e Nazzareno Rossi, ASL 13 in Sondrio e ASL 106 in Teramo. Ciclofosfamide piu’ somatostatina, bromocriptina, retinoidi, melatonina e ACTH nel trattamento dei linfomi non –Hodgkin di basso grado in stadio avanzato: risultati di una
sperimentazione di fase 2. Cancer Biotherapy & Radiopharmaceuticals Volume 16, Number 2, 2001 Mary Ann Liebert, Inc.
67. Turley JM, Funakoshi S, Ruscetti FW, Kasper J, Murphy WJ, Longo DL, et al. Growth inhibition and apoptosis of RL human B lymphoma cells by vitamin E succinate and retinoic acid: role for transforming growth factor beta. Cell Growth Differ. 1995; 6(6): 655-663.
68. Turner HE, Nagy Z, Gatter KC, Esiri MM, Harris AL, Wass JA. Angiogenesis in pituitary adenomas - relationship to endocrine function, treatment and outcome. J Endocrinol. 2000; 165(2): 475-481.
69. Vidal S, Oliveira MC, Kovacs K, Scheithauer BW, Lloyd R. Immunolocalization of vascular endothelial growth factor in the GH3 cell line. Cell Tissue Res. 2000; 300(1): 83-88.
70. Wang C, Tammi M, Guo H, Tammi R.Hyaluronan. Distribution in the normal epithelium of esophagus, stomach, and colon and their cancers.Am J Pathol. 1996 Jun;148(6):1861-9.
71. Wang ZH, Yam HF, Or PC, Yang L . Effects of all-trans-retinoic acid on human esophageal carcinoma cells and their nuclear matrices. Anticancer Res. 1999 Jan-Feb;19(1A):563-8
72. Watson JC, Balster DA, Gebhardt BM, O'Dorisio TM, O'Dorisio MS, Espenan GD, et al. Growing vascular endothelial cells express somatostatin subtype 2 receptors. Br J Cancer. 2001; 85(2): 266-272.
73. Wiedermann CJ, Reinisch N, Braunsteiner H. Stimulation of monocyte chemotaxis by human growth hormone and its deactivation by somatostatin. BZou XN, Taylor PR, Mark SD, lood. 1993; 82(3): 954-960.

